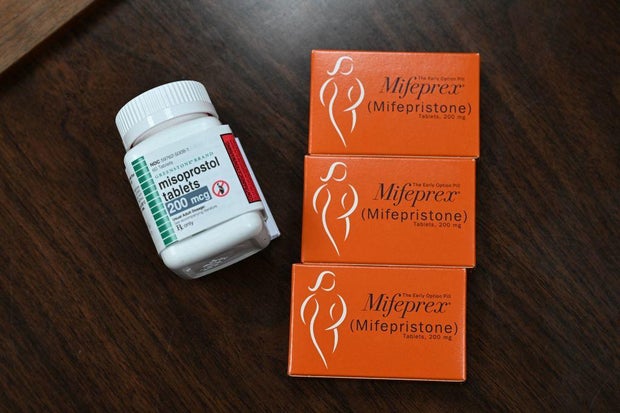
Washington – A Suprema Corte deve se reunir na terça-feira para ouvir argumentos em um caso envolvendo uma pílula abortiva comumente usada e ações recentes da Food and Drug Administration para facilitar a obtenção do medicamento.
No centro da batalha legal está a pílula mifepristona, que é tomada junto com outro medicamento para interromper uma gravidez precoce. Aprovado pela FDA em 2000, mais de 5 milhões de pacientes tomaram mifepristona, de acordo com a agência, e estudos citados em processos judiciais mostraram que é seguro e eficaz.
Nos últimos anos, o FDA tomou uma série de medidas para tornar o mifepristona mais acessível, incluindo permitir que ele seja tomado até 10 semanas de gravidez e entregue pelo correio sem consulta médica pessoal. Essas ações, tomadas em 2016 e 2021, foram submetidas a escrutínio jurídico depois que um grupo de médicos e associações médicas antiaborto alegou que a FDA violou a lei ao flexibilizar as regras.
O Supremo Tribunal está prestes a analisar um decisão de um tribunal federal de apelações que concluiu que as ações da agência eram ilegais. Uma decisão que anulasse essas mudanças ameaçaria restringir o acesso ao mifepristona em todo o país, mesmo em estados com leis que protegem o acesso ao aborto.
O acesso ao mifepristona permaneceu inalterado enquanto os procedimentos legais no caso continuaram, desde que o tribunal superior emitiu uma ordem em abril passado preservando sua disponibilidade. Essa medida permanecerá em vigor até que o Supremo Tribunal emita a sua decisão, prevista para o final de junho.
ROBYN BECK/AFP via Getty Images
As discussões no caso ocorrem menos de dois anos depois que a Suprema Corte decidiu, em junho de 2022, anular o direito constitucional ao aborto e devolver a questão aos estados. E a disputa não é a única envolvendo o aborto que os juízes irão considerar no próximo mês – uma segundo caso envolve se a lei federal exige que médicos de pronto-socorro em estados que proíbem o aborto realizem o procedimento em pacientes grávidas cujas vidas estão em risco.
A consideração do tribunal também surge na sequência de novas descobertas de que os abortos medicamentosos nos EUA aumentaram desde que o Supremo Tribunal revogou o caso Roe v. Wade.
Um estudo publicado segunda-feira na revista médica JAMA descobriu que o número de abortos autogeridos obtidos com o uso de pílulas cresceu nos seis meses após o tribunal superior ter revertido Roe. Uma pesquisa do Instituto Guttmacher, uma organização que apoia o direito ao aborto, publicada na semana passada mostrou que os abortos medicamentosos representaram 63% de todos os abortos ocorridos no sistema de saúde dos EUA em 2023, contra 53% em 2020.
A disputa sobre o mifepristona
A contestação aos esforços da FDA em torno do mifepristona foi apresentada em Novembro de 2022 – mais de duas décadas depois de o medicamento ter sido disponibilizado nos EUA – por um grupo de associações médicas que se opõem ao direito ao aborto. Levados ao tribunal distrital federal do Texas, os grupos, liderados pela Alliance for Hippocratic Medicine, contestaram a aprovação inicial da FDA em 2000 e as suas alterações mais recentes em 2016 e 2021.
Como parte dessas ações, a FDA permitiu que o mifepristona fosse tomado até 10 semanas de gravidez, em vez de sete semanas, reduziu o número de consultas presenciais necessárias de três para uma, permitiu que mais prestadores de cuidados de saúde prescrevessem o medicamento e levantou a exigência de que fosse prescrito pessoalmente.
As organizações, representadas pelo grupo jurídico conservador Alliance Defending Freedom, alegaram que a FDA não tinha autoridade para aprovar a venda do mifepristona e não considerou adequadamente a segurança e eficácia do medicamento.
O juiz federal que supervisiona o caso, o juiz distrital dos EUA Matthew Kacsmaryk, concordou que a aprovação da FDA em 2000 e as ações subsequentes eram provavelmente ilegais. Ele bloqueou a ação inicial do FDA permitindo que o medicamento seja vendido nos EUA
Mas Kacsmaryk suspendeu a sua decisão por uma semana e um tribunal federal de recurso e o Supremo Tribunal intervieram. O tribunal superior finalmente acesso mantido ao mifepristona enquanto o processo judicial prosseguia.
Meses depois, o Tribunal de Apelações do 5º Circuito dos EUA manteve a aprovação do FDA em 2000 da pílula abortiva, mas disse que a agência violou a lei com suas mudanças mais recentes. A decisão do tribunal de recurso, no entanto, foi anulada pela ordem anterior do Supremo Tribunal de Abril de 2023 que protege o acesso.
O Departamento de Justiça e os Laboratórios Danco – o fabricante do Mifeprex, a versão comercial do mifepristona – pediram ao Supremo Tribunal que revisse a decisão do 5º Circuito, e concordou em fazer isso em dezembro.
Os argumentos do caso
Celal Gunes/Anadolu via Getty Images
Ao pedir aos juízes que revertessem a decisão do tribunal de recurso, a administração Biden argumentou que as associações médicas e os seus médicos membros não conseguiram demonstrar que podem ser prejudicados pelas ações da FDA, e que essas alegadas lesões podem ser atribuídas à flexibilização da FDA. das regras do mifepristona.
Os médicos que contestam as mudanças não prescrevem o medicamento e não identificaram um único caso em que um membro tenha sido forçado a realizar um aborto para uma mulher que apareceu em um pronto-socorro com uma gravidez em andamento, disse a procuradora-geral Elizabeth Prelogar ao tribunal. em arquivamentos.
Mas os advogados dos grupos médicos, representados pela Aliança em Defesa da Liberdade, argumentaram que os seus membros se opõem não só ao aborto, mas também à “cumplicidade no processo”.
“A FDA passou décadas encaminhando mulheres prejudicadas por medicamentos abortivos para salas de emergência. Muitos deles procuraram tratamento com os médicos entrevistados”, escreveram os advogados. “Agora que a FDA é chamada a prestar contas pelos danos causados, a agência não pode insistir que a própria opção de tratamento que dirigiu é de alguma forma especulativa”.
Se a Suprema Corte concordar com o Departamento de Justiça que os médicos não têm base adequada para processar no tribunal federal, ordenaria que o caso fosse arquivado sem decidir se a FDA agiu dentro dos limites da lei quando mudou as regras para o uso do mifepristona. .
Mas se os juízes chegarem às questões jurídicas levantadas no caso, o Departamento de Justiça e Danco instaram o tribunal a considerar que as ações da FDA de 2016 e 2021 foram legais.
A agência baseou-se num “volume conjunto de provas médicas” sobre a utilização do mifepristona ao longo de décadas quando determinou que as alterações de 2016 seriam seguras, escreveu Prelogar. De qualquer forma, o tribunal distrital errou ao questionar as determinações que o Congresso autorizou a FDA a tomar, disse ela.
“Até onde é do conhecimento do governo, este caso marca a primeira vez que um tribunal restringe o acesso a um medicamento aprovado pela FDA, questionando a opinião especializada da FDA sobre as condições exigidas para garantir o uso seguro desse medicamento”, escreveu Prelogar.
As empresas farmacêuticas e antigos chefes da FDA alertaram o tribunal que uma decisão que mantém o 5º Circuito ameaça minar o processo de aprovação de medicamentos da agência e pode levar a contestações legais persistentes das suas decisões de aprovação.
A abordagem do tribunal de primeira instância, se deixada intacta, “permitiria aos tribunais substituir a experiência científica da FDA por sua análise leiga e anular a aprovação e as condições de uso da agência para medicamentos – mesmo depois de eles estarem no mercado há décadas”, disse um grupo de ex-comissários e comissários em exercício disseram ao tribunal em um resumo.
“A incerteza resultante ameaçaria os incentivos para as empresas farmacêuticas realizarem o investimento demorado e dispendioso necessário para desenvolver novos medicamentos e, em última análise, dificultaria o acesso dos pacientes a remédios essenciais que previnem o sofrimento e salvam vidas”, afirmaram.
Uma série de empresas farmacêuticas e executivos sublinharam separadamente a importância de as empresas farmacêuticas poderem confiar nos tribunais para respeitarem os julgamentos científicos da FDA.
“Se um tribunal conseguir anular essas decisões muitos anos mais tarde através de um processo desprovido de rigor científico, a incerteza resultante criará riscos intoleráveis e minará os incentivos ao investimento, independentemente do medicamento em questão”, afirmaram num resumo. “Isso, por sua vez, acabará prejudicando os pacientes.”
Mas os advogados das associações médicas e dos seus membros que se opõem ao direito ao aborto argumentaram que a FDA não conseguiu dar uma “explicação satisfatória” para a sua decisão de suspender a exigência de dispensação presencial e qualificou os estudos em que a agência se baseou como “profundamente problemáticos”.
A retirada da exigência de visita presencial em 2021 eliminou a oportunidade dos profissionais de saúde fazerem o rastreio de gravidez ectópica e outras condições, argumentaram as associações. Em 2016, a FDA removeu “salvaguardas inter-relacionadas sem estudos” que examinassem as alterações como um todo, continuaram.
O grupo Americanos Unidos pela Vida, que apoia a Aliança pela Medicina Hipocrática, afirmou que a FDA promoveu o acesso a pílulas abortivas sem supervisão médica, o que aumentou os riscos para a saúde e a segurança das mulheres e interferiu nos seus cuidados.